Với giải Câu 5 trang 47 Hóa học lớp 10 Kết nối tri thức với cuộc sống chi tiết trong Bài 9: Ôn tập chương 2 giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 9: Ôn tập chương 2
Câu 5 trang 47 Hóa học 10: Công thức cấu tạo của phân tử cafein, một chất gây đắng tìm thấy nhiều trong cafe và trà được biểu diễn ở hình bên
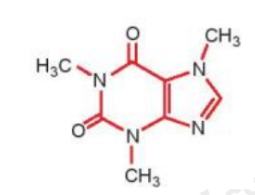
a) Nêu vị trí của các nguyên tố tạo nên cafein trong bảng tuần hoàn.
b) So sánh tính phi kim, bán kính nguyên tử và độ âm điện của các nguyên tố đó và giải thích.
Phương pháp giải:
a) Các nguyên tố tạo nên cafein gồm; N, C, H, O
b)
- Bán kính tăng dần trong một nhóm và giảm dần trong một chu kì.
- Độ âm điện giảm dần trong một nhóm và tăng dần trong một chu kì.
- Tính phi kim giảm dần trong một nhóm và tăng dần trong một chu kì.
- Do H nằm ở một chu kì khác nên dựa vào sự biến đổi trong nhóm I, có nguyên tố Li để làm yếu tố trung gian.
Lời giải:
a)
Nguyên tố H nằm ở ô số 1, chu kì 1, nhóm IA trong bảng tuần hoàn.
Nguyên tố C nằm ở ô số 6, chu kì 2, nhóm IVA trong bảng tuần hoàn.
Nguyên tố N nằm ở ô số 7, chu kì 2, nhóm VA trong bảng tuần hoàn.
Nguyên tố O nằm ở ô số 8, chu kì 2, nhóm VIA trong bảng tuần hoàn.
b)
- Tính phi kim
Trong nhóm IA, tính phi kim giảm dần => tính phi kim H > Li
Trong chu kì 2, tính phi kim tăng dần => O > N > C > Li
=> Tính phi kim của các nguyên tố giảm dần theo thứ tự O, N, C, H
- Bán kính nguyên tử
Trong nhóm IA, bán kính nguyên tử tăng dần => bán kính nguyên tử H < Li
Trong chu kì 2, bán kính nguyên tử giảm dần => O < N < C < Li
=> Bán kính nguyên tử của các nguyên tố tăng dần theo thứ tự H, O, N, C
- Độ âm điện
Trong nhóm IA, độ âm điện giảm dần => độ âm điện H > Li
Trong chu kì 2, độ âm điện tăng dần => O > N > C > Li
=> Độ âm điện của các nguyên tố giảm dần theo thứ tự O > N > C > H
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học